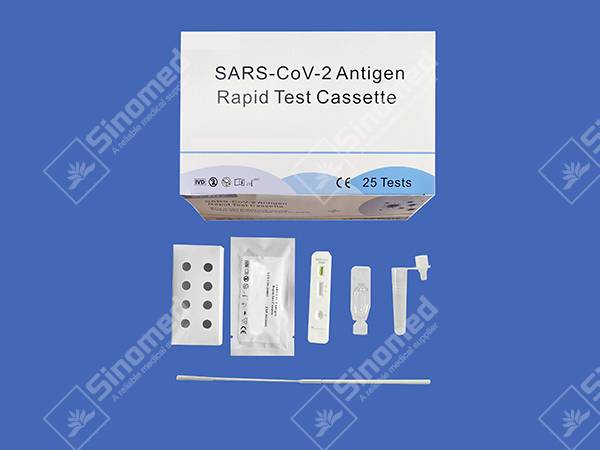
شريط اختبار سريع لمستضد SARS-CoV-2
وصف مختصر:
كاسيت الاختبار السريع لمستضد SARS-CoV-2 هو اختبار مناعي كروماتوجرافي سريع للكشف النوعي عن مستضد SARS-CoV-2 في مسحات البلعوم الأنفي البشري. يعتمد التعريف على الأجسام المضادة وحيدة النسيلة الخاصة ببروتين النوكليوكابسيد (N) لـ SARS-CoV-2. ويهدف إلى المساعدة في التشخيص التفريقي السريع لعدوى COVID-19.
الاستخدام المقصود
الشريط اختبار سريع لمستضد SARS-CoV-2هو اختبار مناعي كروماتوجرافي سريع للكشف النوعي عن مستضد SARS-CoV-2 في مسحات البلعوم الأنفي البشري. يعتمد التعريف على الأجسام المضادة وحيدة النسيلة الخاصة ببروتين النواة (N) لـ SARS-CoV-2. ويهدف إلى المساعدة في التشخيص التفريقي السريع لـكوفيد-19عدوى.
مواصفات الحزمة
25 اختبارًا/عبوة، 50 اختبارًا/عبوة، 100 اختبارًا/عبوة
مقدمة
تنتمي فيروسات كورونا الجديدة إلى جنس β.كوفيد-19هو مرض تنفسي حاد مُعدٍ. عادةً ما يكون الناس عرضة للإصابة به. حاليًا، يُعدّ المصابون بفيروس كورونا المستجد المصدر الرئيسي للعدوى، كما يُمكن أن يكون المصابون الذين لا تظهر عليهم أعراض مصدرًا للعدوى. بناءً على الدراسات الوبائية الحالية، تتراوح فترة حضانة الفيروس بين يوم و14 يومًا، وغالبًا ما تتراوح بين 3 و7 أيام. تشمل الأعراض الرئيسية الحمى والتعب والسعال الجاف. في بعض الحالات، يُلاحظ احتقان الأنف وسيلان الأنف والتهاب الحلق وآلام العضلات والإسهال.
الكواشف
تحتوي أشرطة الاختبار على جزيئات بروتين النوكليوكابسيد المضاد لـ SARS-CoV-2 وبروتين النوكليوكابسيد المضاد لـ SARS-CoV-2 المغلف على الغشاء.
احتياطات
يرجى قراءة كافة المعلومات الموجودة في نشرة العبوة قبل إجراء الاختبار.
١. للاستخدام المهني في التشخيص المختبري فقط. لا يُستخدم بعد تاريخ انتهاء الصلاحية.
2. يجب أن يبقى الاختبار في الكيس المغلق حتى يصبح جاهزًا للاستخدام.
3. يجب اعتبار جميع العينات خطرة محتملة ويجب التعامل معها بنفس الطريقة التي يتم بها التعامل مع عوامل العدوى.
4. يجب التخلص من الاختبار المستخدم وفقًا للوائح المحلية.
5. تجنب استخدام العينات الدموية.
6. ارتدِ القفازات عند التعامل مع العينات، وتجنب لمس غشاء الكاشف والعينة جيدًا.
التخزين والاستقرار
مدة الصلاحية هي 18 شهرًا إذا تم تخزين هذا المنتج في بيئة
2-30 درجة مئوية. يظل الاختبار ثابتًا حتى تاريخ انتهاء الصلاحية المطبوع على الكيس المختوم. يجب أن يظل الاختبار في الكيس المختوم حتى الاستخدام.لا تجمد.لا تستخدم بعد تاريخ انتهاء الصلاحية.
جمع العينات وتحضيرها
1. جمع إفرازات الحلق: إدخال مسحة معقمة إلى الحلق بالكامل من الفم، مع التركيز على جدار الحلق والمنطقة المحمرة من اللوزتين الحنكية، ومسح اللوزتين البلعوميتين الثنائيتين وجدار البلعوم الخلفي بمسحة معتدلة.
القوة، تجنب لمس اللسان وأخرج المسحة.
٢. عالج العينة فورًا بمحلول استخلاص العينة المرفق مع المجموعة بعد جمعها. إذا تعذر ذلك فورًا، فيجب تخزين العينة في أنبوب بلاستيكي جاف ومعقم ومحكم الغلق. يمكن تخزينها في درجة حرارة تتراوح بين ٢ و٨ درجات مئوية لمدة ٨ ساعات، ويمكن تخزينها لفترة طويلة في درجة حرارة -٧٠ درجة مئوية.
٣. لا يُنصح باستخدام العينات الملوثة بشدة ببقايا الطعام الفموي لاختبار هذا المنتج. لا يُنصح باستخدام العينات المأخوذة من مسحات شديدة اللزوجة أو متكتلة لاختبار هذا المنتج. إذا كانت المسحات ملوثة بكمية كبيرة من الدم، فلا يُنصح باستخدامها لاختبار هذا المنتج. لا يُنصح باستخدام العينات التي تمت معالجتها بمحلول استخلاص عينات غير مُرفق في هذه المجموعة لاختبار هذا المنتج.
مكونات المجموعة
توفير المواد
| أشرطة الاختبار | كاشف الاستخلاص | أنابيب الاستخراج | |
| مسحات معقمة | نشرة الحزمة | محطة العمل |
المواد المطلوبة ولكن غير متوفرة
| المؤقت | للاستخدام التوقيتي. |
| طَرد |
المواصفات25
الاختبارات/حزمة 50
الاختبارات/الحزمة 100
اختبارات/حزمة كاشف استخلاص العينات 25 اختبارًا/حزمة 50 اختبارًا/حزمة 100 اختبار/حزمة استخلاص العينات
أنبوب ≥25 اختبارًا/عبوة ≥50 اختبارًا/عبوة ≥100 اختبار/عبوة التعليمات راجع
الحزمة راجع
الحزمة راجع
طَرد
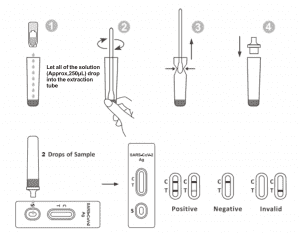
طريقة الاستخدام
اسمح للاختبار والعينة ومحلول الاستخراج بالتوازن مع درجة حرارة الغرفة (15-30 درجة مئوية) قبل الاختبار.
1. أخرج شريط الاختبار من الكيس المغلق واستخدمه خلال 15 دقيقة. ستحصل على أفضل النتائج بإجراء الاختبار فور فتح الكيس.
2. ضع أنبوب الاستخلاص في محطة العمل. أمسك زجاجة الكاشف الاستخلاص رأسًا على عقب. اضغط على الزجاجة واترك كل المحلول (حوالي 250 ميكرولترًا) يسقط في أنبوب الاستخلاص بحرية دون لمس حافة الأنبوب بأنبوب الاستخلاص.
3. ضع عينة المسحة في أنبوب الاستخلاص. قم بتدوير المسحة لمدة 10 ثوانٍ تقريبًا أثناء الضغط على الرأس على الجزء الداخلي من الأنبوب لتحرير المستضد الموجود في المسحة.
4. قم بإزالة المسحة مع الضغط على رأس المسحة على الجزء الداخلي من أنبوب الاستخراج أثناء إزالتها لإخراج أكبر قدر ممكن من السائل من المسحة. تخلص من المسحة وفقًا لبروتوكول التخلص من النفايات البيولوجية الخطرة لديك.
5. قم بتركيب طرف القطارة أعلى أنبوب الاستخلاص. ضع شريط الاختبار على سطح نظيف ومستو.
6. أضف قطرتين من المحلول (حوالي 65 ميكرولترًا) إلى بئر العينة ثم ابدأ تشغيل المؤقت. اقرأ النتيجة المعروضة في غضون 20-30 دقيقة، والنتائج المقروءة بعد 30 دقيقة غير صالحة.
تفسير النتائج
| سلبي نتيجة: |
يظهر خط ملون واحد في منطقة خط التحكم (ج). لا يظهر أي خط في منطقة الاختبار (ت). تشير النتيجة السلبية إلى عدم وجود مستضد فيروس كورونا المستجد-2 (SARS-CoV-2) في العينة، أو وجوده أقل من المستوى القابل للكشف في الاختبار.
إيجابينتيجة:
يظهر خطان. يجب أن يكون أحد الخطين الملونين في منطقة التحكم (C) ويجب أن يكون الخط الملون الظاهر الآخر في منطقة الاختبار (T). تشير النتيجة الإيجابية إلى أنه تم اكتشاف SARS-CoV-2 في العينة.
نتيجة غير صالحة:
فشل خط التحكم. غالبًا ما يكون سبب فشل خط التحكم هو عدم كفاية حجم العينة أو اتباع أساليب إجرائية خاطئة. راجع الإجراء وأعد الاختبار باختبار جديد. إذا استمرت المشكلة، فتوقف عن استخدام مجموعة الاختبار فورًا واتصل بالموزع المحلي.
ملحوظة:
تختلف شدة اللون في منطقة خط الاختبار (T) تبعًا لتركيز مستضد فيروس كورونا المستجد (SARS-CoV-2) الموجود في العينة. لذلك، يُعتبر أي لون في منطقة خط الاختبار (T) إيجابيًا.
ضبط الجودة
- يتضمن الاختبار عنصر تحكم إجرائي. يُعتبر ظهور خط ملون في منطقة التحكم (ج) عنصر تحكم إجرائي داخلي. ويؤكد هذا وجود فتيل غشاء كافٍ.
- لا يتم توفير معايير التحكم مع هذه المجموعة؛ ومع ذلك، يوصى باختبار عناصر التحكم الإيجابية والسلبية كممارسة معملية جيدة لتأكيد إجراء الاختبار والتحقق من أداء الاختبار المناسب.
القيودمن الاختبار
- شريط اختبار مستضد SARS-CoV-2 السريع مخصص للاستخدام التشخيصي المهني في المختبر فقط. يجب استخدام الاختبار للكشف عن مستضد SARS-CoV-2 في مسحة البلعوم الفموي. لا يمكن تحديد القيمة الكمية أو معدل الزيادة في تركيز SARS-CoV-2 من خلال هذا الاختبار النوعي.
- تعتمد دقة الاختبار على جودة عينة المسحة. قد تؤدي عملية تخزين العينة بشكل غير صحيح إلى نتائج سلبية خاطئة.
- سيشير شريط الاختبار السريع لمستضد SARS-CoV-2 فقط إلى وجود SARS-CoV-2 في العينة من سلالات فيروس كورونا SARS-CoV-2 القابلة للحياة وغير القابلة للحياة.
- كما هو الحال مع جميع الاختبارات التشخيصية، يجب تفسير جميع النتائج مع المعلومات السريرية الأخرى المتاحة للطبيب.
- يجب تأكيد النتيجة السلبية التي تم الحصول عليها من هذه المجموعة عن طريق اختبار تفاعل البوليميراز المتسلسل (PCR). يمكن الحصول على نتيجة سلبية إذا كان تركيز SARS-CoV-2 الموجود في المسحة غير كافٍ أو كان أقل من المستوى القابل للكشف عنه في الاختبار.
- قد يتداخل وجود كمية زائدة من الدم أو المخاط في عينة المسحة مع الأداء وقد يؤدي إلى نتيجة إيجابية خاطئة.
- النتيجة الإيجابية لفيروس كورونا المستجد (SARS-CoV-2) لا تستبعد وجود عدوى بكتيرية كامنة. لذلك، ينبغي الأخذ في الاعتبار احتمالية وجود عدوى بكتيرية كامنة.
- النتائج السلبية لا تستبعد الإصابة بفيروس كورونا المستجد (SARS-CoV-2)، خاصةً لدى الأشخاص الذين كانوا على اتصال مباشر بالفيروس. ينبغي النظر في إجراء فحص متابعة مع تشخيص جزيئي لاستبعاد الإصابة لدى هؤلاء الأفراد.
- قد تكون النتائج الإيجابية بسبب وجود عدوى بسلالات فيروس كورونا غير SARS-CoV-2، مثل فيروس كورونا HKU1، أو NL63، أو OC43، أو 229E.
- لا ينبغي استخدام نتائج اختبار المستضد كأساس وحيد لتشخيص أو استبعاد الإصابة بفيروس SARS-CoV-2 أو لإبلاغ حالة الإصابة.
- لدى كاشف الاستخلاص القدرة على قتل الفيروس، لكنه لا يستطيع تعطيل 100% من الفيروس. يمكن الرجوع إلى طريقة تعطيل الفيروس: ما هي الطريقة التي أوصت بها منظمة الصحة العالمية/مراكز السيطرة على الأمراض والوقاية منها، أو يمكن التعامل معها وفقًا للوائح المحلية.
خصائص الأداء
حساسيةوالخصوصية
تم تقييم شريط اختبار مستضد SARS-CoV-2 السريع باستخدام العينات التي تم الحصول عليها من المرضى. يتم استخدام تفاعل البوليميراز المتسلسل (PCR) كطريقة مرجعية لشريط اختبار مستضد SARS-CoV-2 السريع. تم اعتبار العينات إيجابية إذا أشار تفاعل البوليميراز المتسلسل (PCR) إلى نتيجة إيجابية.
| طريقة | تفاعل البوليميراز المتسلسل العكسي العكسي | النتائج الإجمالية | ||
| شريط اختبار سريع لمستضد SARS-CoV-2 | نتائج | إيجابي | سلبي | |
| إيجابي | 38 | 3 | 41 | |
| سلبي | 2 | 360 | 362 | |
| النتائج الإجمالية | 40 | 363 | 403 | |
الحساسية النسبية: 95.0%(95%CI*:83.1%-99.4%)
الخصوصية النسبية: 99.2% (95%CI*:97.6%-99.8%)
*فواصل الثقة
حد الكشف
عندما يكون محتوى الفيروس أكبر من 400TCID50/مل، معدل الكشف الإيجابي أكبر من 95%. عندما يكون محتوى الفيروس أقل من 200TCID50/مل، معدل الكشف الإيجابي أقل من 95%، وبالتالي فإن الحد الأدنى للكشف لهذا المنتج هو 400TCID50/مل.
دقة
تم اختبار دقة ثلاث دفعات متتالية من الكواشف. استُخدمت دفعات مختلفة من الكواشف لاختبار العينة السلبية نفسها عشر مرات متتالية، وكانت جميع النتائج سلبية. استُخدمت دفعات مختلفة من الكواشف لاختبار العينة الإيجابية نفسها عشر مرات متتالية، وكانت جميع النتائج إيجابية.
تأثير الخطاف
عندما يصل محتوى الفيروس في العينة المراد اختبارها إلى 4.0*105معرف مركز التحكم50/مل، نتيجة الاختبار لا تزال لا تظهر تأثير HOOK.
التفاعل المتبادل
تم تقييم التفاعل المتبادل للمجموعة. أظهرت النتائج عدم وجود أي تفاعل متبادل مع العينة التالية.
| اسم | تركيز |
| فيروس التهاب الكبد الوبائي HCOV-HKU1 | 105معرف مركز التحكم50/مل |
| المكورات العنقودية الذهبية | 106معرف مركز التحكم50/مل |
| العقديات المجموعة أ | 106معرف مركز التحكم50/مل |
| فيروس الحصبة | 105معرف مركز التحكم50/مل |
| فيروس النكاف | 105معرف مركز التحكم50/مل |
| الفيروس الغدي من النوع 3 | 105معرف مركز التحكم50/مل |
| الالتهاب الرئوي الميكوبلازما | 106معرف مركز التحكم50/مل |
| فيروس بارايمفلونزا من النوع 2 | 105معرف مركز التحكم50/مل |
| فيروس ميتا نيمو البشري | 105معرف مركز التحكم50/مل |
| فيروس كورونا البشري OC43 | 105معرف مركز التحكم50/مل |
| فيروس كورونا البشري 229E | 105معرف مركز التحكم50/مل |
| بورديتيلا بارابيرتوسيس | 106معرف مركز التحكم50/مل |
| سلالة إنفلونزا ب فيكتوريا | 105معرف مركز التحكم50/مل |
| سلالة الإنفلونزا ب | 105معرف مركز التحكم50/مل |
| إنفلونزا A H1N1 2009 | 105معرف مركز التحكم50/مل |
| إنفلونزا A H3N2 | 105معرف مركز التحكم50/مل |
| H7N9 | 105معرف مركز التحكم50/مل |
| H5N1 | 105معرف مركز التحكم50/مل |
| فيروس إبشتاين بار | 105معرف مركز التحكم50/مل |
| الفيروس المعوي CA16 | 105معرف مركز التحكم50/مل |
| فيروس الراينو | 105معرف مركز التحكم50/مل |
| الفيروس المخلوي التنفسي | 105معرف مركز التحكم50/مل |
| العقدية الرئوية | 106معرف مركز التحكم50/مل |
| المبيضات البيضاء | 106معرف مركز التحكم50/مل |
| الكلاميديا الرئوية | 106معرف مركز التحكم50/مل |
| بورديتيلا السعال الديكي | 106معرف مركز التحكم50/مل |
| المتكيسة الرئوية الجيروفيشية | 106معرف مركز التحكم50/مل |
| المتفطرة السلية | 106معرف مركز التحكم50/مل |
| ليجيونيلا نيوموفيلا | 106معرف مركز التحكم50/مل |
Iالمواد المتداخلة
لا يجوز التدخل في نتائج الاختبار بالمادة عند التركيز التالي:
| التدخل مادة | مركز | المادة المتداخلة | مركز |
| الدم الكامل | 4% | جل البنزوين المركب | 1.5 ملغ/مل |
| ايبوبروفين | 1 ملغ/مل | كرومولين جليكات | 15% |
| التتراسيكلين | 3 ميكروغرام/مل | الكلورامفينيكول | 3 ميكروغرام/مل |
| المخاط | 0.5% | موبيروسين | 10 ملغ/مل |
| إريثروميسين | 3 ميكروغرام/مل | أوسيلتاميفير | 5 ملغ/مل |
| توبراميسين | 5% | قطرات نافازولين هيدروكلوريد الأنفية | 15% |
| المنثول | 15% | رذاذ بروبيونات فلوتيكازون | 15% |
| عفرين | 15% | هيدروكلوريد ديوكسي إبينفرين | 15% |
قائمة المراجع
1. فايس س.ر.، ليبوفيتز ج.ز. مسببات أمراض فيروس كورونا. مجلة أبحاث الفيروسات المتقدمة 2011؛ 81: 85-164
2.Cui J، Li F، Shi ZL. أصل وتطور فيروسات كورونا المسببة للأمراض.Nat Rev Microbiol 2019؛ 17: 181-192.
٣. سو إس، وونغ جي، وشي دبليو، وآخرون. علم الأوبئة، وإعادة التركيب الجيني، والتسبب في أمراض فيروسات كورونا. تريندز ميكروبيول ٢٠١٦؛ ٢٤: ٤٩٠-٥٠٢.