COVID-19 IgG/IgM-Schnelltestkassette
Kurze Beschreibung:
Bei der COVID-19 IgG/IgM-Schnelltestkassette handelt es sich um einen Lateral-Flow-Immunoassay zum qualitativen Nachweis von IgG- und IgM-Antikörpern gegen das SARS-CoV-2-Virus in Vollblut-, Serum- oder Plasmaproben von Personen, bei denen von ihrem Arzt der Verdacht auf eine COVID-19-Infektion besteht.
Der CO VID-19 IgG/IgM-Schnelltest unterstützt die Diagnose von Patienten mit Verdacht auf eine SARS -CoV-2-Infektion in Verbindung mit dem klinischen Bild und den Ergebnissen anderer Labortests. Er wird als ergänzender Testindikator bei Verdachtsfällen mit negativem Nukleinsäuretest auf das neuartige Coronavirus oder in Verbindung mit einem Nukleinsäuretest bei Verdachtsfällen empfohlen. Ergebnisse von Antikörpertests sollten nicht als alleinige Grundlage für die Diagnose oder den Ausschluss einer SARS -CoV-2-Infektion oder zur Bestimmung des Infektionsstatus verwendet werden.
Negative Ergebnisse schließen eine SARS -CoV-2-Infektion nicht aus, insbesondere bei Personen, die Kontakt zu bekanntermaßen infizierten Personen hatten oder sich in Gebieten mit hoher Prävalenz aktiver Infektionen aufgehalten haben. Um bei diesen Personen eine Infektion auszuschließen, sollten Folgetests mit einem molekulardiagnostischen Verfahren in Betracht gezogen werden.
Positive Ergebnisse können auf eine frühere oder gegenwärtige Infektion mit Nicht-SARS-CoV-2-Coronavirus-Stämmen zurückzuführen sein.
Der Test ist für die Verwendung in klinischen Labors oder durch medizinisches Personal am Point-of-Care vorgesehen und nicht für den Heimgebrauch. Der Test sollte nicht zum Screening von gespendetem Blut verwendet werden.
Nur für den professionellen und In-vitro-Diagnostikgebrauch.
Nur für den professionellen und In-vitro-Diagnostikgebrauch.
VERWENDUNGSZWECK
DerCOVID-19 IgG/IgM-Schnelltestkassetteist ein Lateral-Flow-Immunoassay, der für den qualitativen Nachweis von IgG- und IgM-Antikörpern gegen das SARS-CoV-2-Virus in Vollblut-, Serum- oder Plasmaproben von Personen entwickelt wurde, bei denen von ihrem Arzt der Verdacht auf eine COVID-19-Infektion besteht.
Der CO VID-19 IgG/IgM-Schnelltest unterstützt die Diagnose von Patienten mit Verdacht auf eine SARS -CoV-2-Infektion in Verbindung mit dem klinischen Bild und den Ergebnissen anderer Labortests. Er wird als ergänzender Testindikator bei Verdachtsfällen mit negativem Nukleinsäuretest auf das neuartige Coronavirus oder in Verbindung mit einem Nukleinsäuretest bei Verdachtsfällen empfohlen. Ergebnisse von Antikörpertests sollten nicht als alleinige Grundlage für die Diagnose oder den Ausschluss einer SARS -CoV-2-Infektion oder zur Bestimmung des Infektionsstatus verwendet werden.
Negative Ergebnisse schließen eine SARS -CoV-2-Infektion nicht aus, insbesondere bei Personen, die Kontakt zu bekanntermaßen infizierten Personen hatten oder sich in Gebieten mit hoher Prävalenz aktiver Infektionen aufgehalten haben. Um bei diesen Personen eine Infektion auszuschließen, sollten Folgetests mit einem molekulardiagnostischen Verfahren in Betracht gezogen werden.
Positive Ergebnisse können auf eine frühere oder gegenwärtige Infektion mit Nicht-SARS-CoV-2-Coronavirus-Stämmen zurückzuführen sein.
Der Test ist für die Verwendung in klinischen Labors oder durch medizinisches Personal am Point-of-Care vorgesehen und nicht für den Heimgebrauch. Der Test sollte nicht zum Screening von gespendetem Blut verwendet werden.
ZUSAMMENFASSUNG
Die neuartigen Coronaviren gehören zur Gattung P.COVID 19ist eine akute Infektionskrankheit der Atemwege. Jeder Mensch ist anfällig. Derzeit sind mit dem neuen Coronavirus infizierte Patienten die Hauptinfektionsquelle; auch asymptomatische Personen können eine Infektionsquelle darstellen. Nach aktuellen epidemiologischen Untersuchungen beträgt die Inkubationszeit 1 bis 14 Tage, meist 3 bis 7 Tage. Zu den Hauptsymptomen gehören Fieber, Müdigkeit und trockener Husten. Verstopfte Nase, Schnupfen, Halsschmerzen, Myalgie und Durchfall treten in einigen Fällen auf.
Wenn das SARS-CoV-2-Virus einen Organismus infiziert, ist RNA, das genetische Material des Virus, der erste nachweisbare Marker. Das Viruslastprofil von SARS-CoV-2 ähnelt dem der Grippe. Es erreicht seinen Höhepunkt etwa zum Zeitpunkt des Symptombeginns und beginnt dann abzufallen. Im weiteren Krankheitsverlauf nach der Infektion produziert das menschliche Immunsystem Antikörper. IgM ist der frühe Antikörper, der vom Körper nach der Infektion produziert wird und die akute Phase der Infektion anzeigt. IgG-Antikörper gegen SARS-CoV2 werden später nach der Infektion nachweisbar. Positive Ergebnisse sowohl für IgG als auch für IgM können nach der Infektion auftreten und auf eine akute oder kürzlich erfolgte Infektion hinweisen. IgG weist auf die Rekonvaleszenzphase der Infektion oder eine frühere Infektion hin.
Sowohl IgM als auch IgG haben jedoch ein Zeitfenster zwischen der Virusinfektion und der Antikörperproduktion. IgM tritt fast erst mehrere Tage nach Ausbruch der Krankheit auf, sodass ihr Nachweis oft hinter dem Nukleinsäurenachweis zurückbleibt und weniger empfindlich ist als der Nukleinsäurenachweis. In Fällen, in denen Nukleinsäureamplifikationstests negativ sind und ein starker epidemiologischer Zusammenhang bestehtCOVID 19Infektion könnten gepaarte Serumproben (in der akuten und Rekonvaleszenzphase) die Diagnose unterstützen.
PRINZIP
Die COVID-19 IgG/IgM-Schnelltestkassette (WB/S/P) ist ein qualitativer Membranstreifen-basierter Immunoassay zum Nachweis von Antikörpern (IgG und IgM) gegen das neuartige Coronavirus in menschlichem Vollblut/Serum/Plasma. Die Testkassette besteht aus:1) ein burgunderfarbenes Koiyugate-Pad mit rekombinanten Hüllantigenen des neuartigen Coronavirus, koi^ugiert mit kolloidalem Gold (neuartiges Coronavirus c两ugates), 2) ein Nitrozellulosemembranstreifen mit zwei Testlinien (IgG- und IgM-Linien) und einer Kontrolllinie (C-Linie). Die IgM-Linie ist mit dem Maus-Anti-Human-IgM-Antikörper vorbeschichtet, die IgG-Linie ist mit dem Maus-Anti-Human-IgG-Antikörper beschichtet, wenn ein angemessenes Volumen der letzten Probe in die Probenvertiefung der Testkassette gegeben wird. Die Probe wandert durch Kapillarwirkung durch die Kassette. IgM gegen das neuartige Coronavirus, falls in der Probe vorhanden, bindet an die Konjugate des neuartigen Coronavirus. Der Immunkomplex wird dann durch das auf dem IgM-Band vorbeschichtete Reagenz eingefangen und bildet eine burgunderfarbene IgM-Linie, die ein positives Testergebnis für das neuartige Coronavirus IgM anzeigt. IgG gegen das neuartige Coronavirus, falls in der Probe vorhanden, bindet an die Konjugate des neuartigen Coronavirus. Der Immunkomplex wird dann durch das auf der IgG-Linie beschichtete Reagenz erfasst und bildet eine burgunderfarbene IgG-Linie, die ein positives Testergebnis für das neuartige Coronavirus IgG anzeigt. Das Fehlen jeglicher T-Linien (IgG und IgM) deutet auf eine
negatives Ergebnis. Zur Verfahrenskontrolle erscheint im Kontrolllinienbereich immer eine farbige Linie, die anzeigt, dass die richtige Probenmenge hinzugefügt wurde und eine Dochtwirkung auf die Membran stattgefunden hat.
WARNHINWEISE UND VORSICHTSMASSNAHMEN
- Nur zur In-vitro-Diagnostik.
- Für medizinisches Fachpersonal und professionelle Point-of-Care-Standorte.
• Nach Ablauf des Verfallsdatums nicht mehr verwenden.
- Bitte lesen Sie alle Informationen in dieser Packungsbeilage, bevor Sie den Test durchführen. •Die Testkassette sollte bis zur Verwendung im versiegelten Beutel bleiben.
•Alle Proben sollten als potenziell gefährlich betrachtet und auf die gleiche Weise wie ein Infektionserreger behandelt werden.
•Die gebrauchte Testkassette sollte gemäß den bundesstaatlichen, staatlichen und örtlichen Vorschriften entsorgt werden.
ZUSAMMENSETZUNG
Der Test enthält einen Membranstreifen, der mit Maus-Anti-Human-IgM-Antikörpern und Maus-Anti-Human-IgG-Antikörpern beschichtet ist.
Testlinie und ein Farbkissen, das kolloidales Gold in Verbindung mit rekombinantem Antigen des neuartigen Coronavirus enthält. Die Anzahl der Tests ist auf dem Etikett aufgedruckt.
Mitgelieferte Materialien
- Testkassette • Packungsbeilage
- Puffer • Tropfer
- Lanzette
Benötigte, aber nicht mitgelieferte Materialien
•Probensammelbehälter • Timer
LAGERUNG UND STABILITÄT
• Wie verpackt im versiegelten Beutel bei einer Temperatur von 4–30 °F oder 40–86 °F lagern. Das Kit ist bis zum auf dem Etikett aufgedruckten Verfallsdatum stabil.
• Nach dem Öffnen des Beutels sollte das Produkt innerhalb einer Stunde verbraucht werden. Längerer Kontakt mit heißen und feuchten Umgebungen führt zur Verschlechterung der Produktqualität.
• Die Charge und das Verfallsdatum wurden auf der Kennzeichnung SPECIMEN aufgedruckt
•Der Test kann zum Testen von Vollblut-/Serum-/Plasmaproben verwendet werden.
• Zur Entnahme von Vollblut-, Serum- oder Plasmaproben gemäß den üblichen klinischen Laborverfahren.
• Trennen Sie Serum oder Plasma so schnell wie möglich vom Blut, um eine Hämolyse zu vermeiden. Verwenden Sie nur klare, nicht hämolysierte Proben.
• Proben bei 2–8 °C (36–46 °F) lagern, wenn sie nicht sofort getestet werden. Bei 2–8 °C bis zu 7 Tage lagern. Für eine längere Lagerung sollten die Proben bei -20 °C (-4 °F) eingefroren werden. Vollblutproben nicht einfrieren.、
• Vermeiden Sie mehrere Gefrier- und Auftauzyklen. Bringen Sie gefrorene Proben vor dem Test langsam auf Raumtemperatur und mischen Sie sie vorsichtig.
Proben, die sichtbare Partikel enthalten, sollten vor dem Test durch Zentrifugation geklärt werden.
•Verwenden Sie keine Proben, die eine starke Lipämie, eine starke Hämolyse oder eine Trübung aufweisen, um Störungen bei der Ergebnisinterpretation zu vermeiden.
TESTVERFAHREN
Lassen Sie das Testgerät und die Proben vor dem Test auf die richtige Temperatur (15–30 °C oder 59–86 °T) abkühlen.
- Nehmen Sie die Testkassette aus dem versiegelten Beutel.
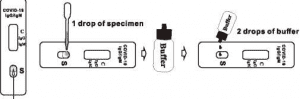
- Halten Sie die Pipette senkrecht und geben Sie 1 Tropfen (ca. 10 µl) der Probe in den oberen Bereich der Probenvertiefung(en). Achten Sie dabei darauf, dass keine Luftblasen entstehen. Für eine höhere Genauigkeit verwenden Sie eine Pipette mit einem Volumen von 10 µl. Siehe Abbildung unten.
- Geben Sie dann sofort 2 Tropfen (ca. 70 µl) Puffer in die Probenvertiefung(en).
- Starten Sie den Timer.
- bis farbige Linien erscheinen. Interpretieren Sie die Testergebnisse nach 15 Minuten. Lesen Sie die Ergebnisse nicht nach 20 Minuten ab.
Bereich für Proben
(Das Bild dient nur als Referenz, bitte beziehen Sie sich auf das Materialobjekt.)
INTERPRETATION DER ERGEBNISSE
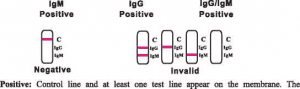
Antikörper. Das Auftreten der IgM-Testlinie weist auf das Vorhandensein von für das neue Coronavirus spezifischen IgM-Antikörpern hin. Erscheinen sowohl die IgG- als auch die IgM-Linie, weist dies auf das Vorhandensein sowohl von für das neue Coronavirus spezifischen IgG- als auch IgM-Antikörpern hin.
Negativ:Im Kontrollbereich (C) erscheint eine farbige Linie. Im Testlinienbereich erscheint keine sichtbare farbige Linie.
Ungültig:Die Kontrolllinie wird nicht angezeigt. Unzureichendes Probenvolumen oder falsche Verfahrenstechniken sind die wahrscheinlichsten Gründe für das Versagen der Kontrolllinie. Überprüfen Sie den Vorgang und wiederholen Sie den Test mit einer neuen Testkassette. Sollte das Problem weiterhin bestehen, stellen Sie die Verwendung des Testkits sofort ein und wenden Sie sich an Ihren lokalen Händler.
QUALITÄTSKONTROLLE
Der Test beinhaltet eine Verfahrenskontrolle. Eine farbige Linie im Kontrollbereich (C) gilt als interne Verfahrenskontrolle. Sie bestätigt ausreichendes Probenvolumen, ausreichende Membrandurchdringung und korrekte Verfahrenstechnik. Kontrollstandards sind nicht im Lieferumfang enthalten. Es wird jedoch empfohlen, Positiv- und Negativkontrollen im Rahmen guter Laborpraxis zu testen, um das Testverfahren zu bestätigen und die ordnungsgemäße Testdurchführung zu überprüfen.
EINSCHRÄNKUNGEN
• Die COVID-19 IgG/IgM-Schnelltestkassette (WB/S/P) ist auf die Bereitstellung einer qualitativen
Nachweis. Die Intensität der Testlinie korreliert nicht unbedingt mit der Antikörperkonzentration im Blut. Die Ergebnisse dieses Tests dienen lediglich der Diagnose. Jeder Arzt muss die Ergebnisse im Zusammenhang mit der Patientenanamnese, den körperlichen Befunden und anderen diagnostischen Verfahren interpretieren.
• Ein negatives Testergebnis zeigt an, dass Antikörper gegen das neuartige Coronavirus entweder nicht vorhanden sind oder in Konzentrationen vorliegen, die durch den Test nicht nachweisbar sind.
LEISTUNGSMERKMALE
Genauigkeit
Zusammenfassende Daten des CO VID-19 IgG/IgM-Schnelltests wie unten
Bezüglich des IgG-Tests haben wir die Positivrate der 82 Patienten während der Rekonvaleszenzzeit gezählt.
COVID-19 IgG:
| COVID-19 IgG | Anzahl der Patienten während der Rekonvaleszenz | Gesamt |
| Positiv | 80 | 80 |
| Negativ | 2 | 2 |
| Gesamt | 82 | 82 |
Die Ergebnisse ergaben eine Sensitivität von 97,56 %
Bezüglich des IgM-Tests erfolgt der Ergebnisvergleich mit der RT-PCR.
COVID-19 IgM:
| COVID-19 IgM | RT-PCR | Gesamt | |
| Positiv | Negativ | ||
| Positiv | 70 | 2 | 72 |
| Negativ | 9 | 84 | 93 |
| Gesamt | 79 | 86 | 165 |
Ein statistischer Vergleich der Ergebnisse ergab eine Sensitivität von 88,61 %, eine Spezifität von 97,67 % und eine Genauigkeit von 93,33 %.
Kreuzreaktivität und Interferenz
1. Andere häufige Erreger von Infektionskrankheiten wurden auf Kreuzreaktivität mit dem Test untersucht. Einige positive Proben anderer häufiger Infektionskrankheiten wurden zu den positiven und negativen Proben des neuen Coronavirus gegeben und separat getestet. Es wurde keine Kreuzreaktivität mit Proben von Patienten beobachtet, die mit HIV, HA, HBsAg, HCV TP, HTIA, CMV FLUA, FLUB, RSy MP, CP oder HPIV infiziert waren.
2.Potenziell kreuzreaktive endogene Substanzen, einschließlich gängiger Serumbestandteile wie Lipide, Hämoglobin und Bilirubin, wurden in hohen Konzentrationen in die positiven und negativen Proben des neuen Coronavirus eingebracht und separat getestet.
Es wurden keine Kreuzreaktivität oder Interferenzen mit dem Gerät beobachtet.
| Analyten | Kegel. | Proben | |
| Positiv | Negativ | ||
| Albumin | 20 mg/ml | + | |
| Bilirubin | 20 p,g/ml | + | |
| Hämoglobin | 15 mg/ml | + | |
| Glucose | 20 mg/ml | + | |
| Harnsäure | 200 g/ml | + | |
| Lipide | 20 mg/ml | + | |
3. Einige andere gängige biologische Analyten wurden den positiven und negativen Proben für das neuartige Coronavirus zugesetzt und separat getestet. Bei den in der folgenden Tabelle aufgeführten Konzentrationen wurden keine signifikanten Interferenzen beobachtet.
| Analyten | Konz. (gg/ ml) | Proben | |
| Positiv | Negativ | ||
| Acetessigsäure | 200 | + | |
| Acetylsalicylsäure | 200 | + | |
| Benzoylecgonin | 100 | + | |
| Koffein | 200 | + | |
| EDTA | 800 | + | |
| Ethanol | 1,0 % | + | |
| Gentisinsäure | 200 | + | |
| p-Hydroxybutyrat | 20.000 | + | |
| Methanol | 10,0 % | + | |
| Phenothiazin | 200 | + | |
| Phenylpropanolamin | 200 | + | |
| Salicylsäure | 200 | + | |
| Acetaminophen | 200 | + | |
Reproduzierbarkeit
In drei Arztpraxen wurden Reproduzierbarkeitsstudien für den IgG/IgM-Schnelltest auf das neuartige Coronavirus durchgeführt. 60 klinische Serumproben, davon 20 negative, 20 grenzwertig positive und 20 positive, wurden für diese Studie verwendet. Jede Probe wurde in dreifacher Ausführung drei Tage lang in den jeweiligen Arztpraxen getestet. Die Übereinstimmung innerhalb der Tests betrug 100 %. Die Übereinstimmung zwischen den Standorten betrug ebenfalls 100 %.