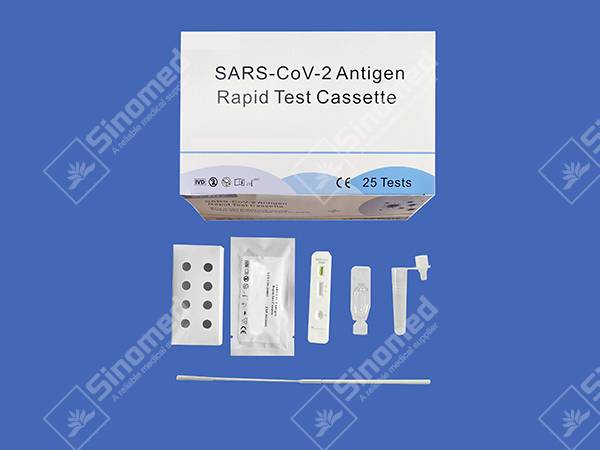
Kaset Tes Cepat Antigen SARS-CoV-2
Deskripsi Singkat:
Kaset Tes Cepat Antigen SARS-CoV-2 adalah immunoassay kromatografi cepat untuk deteksi kualitatif antigen SARS-CoV-2 pada usap Orofaring manusia. Identifikasi didasarkan pada antibodi monoklonal spesifik untuk Protein Nukleokapsid (N) SARS- CoV-2.Hal ini dimaksudkan untuk membantu diagnosis banding infeksi COVID-19 secara cepat.
PENGGUNAAN YANG DIMAKSUDKAN
ItuKaset Tes Cepat Antigen SARS-CoV-2adalah immunoassay kromatografi cepat untuk deteksi kualitatif antigen SARS-CoV-2 pada usap Orofaring manusia. Identifikasi didasarkan pada antibodi monoklonal spesifik untuk Protein Nukleokapsid (N) SARS-CoV-2. Hal ini dimaksudkan untuk membantu dalam diagnosis banding yang cepatCOVID 19infeksi.
Spesifikasi Paket
25 tes/paket, 50 tes/paket, 100 tes/paket
PERKENALAN
Virus corona baru termasuk dalam genus β.COVID 19adalah penyakit infeksi pernafasan akut. Masyarakat pada umumnya rentan. Saat ini, pasien yang terinfeksi virus corona baru merupakan sumber utama penularan; orang yang terinfeksi tanpa gejala juga dapat menjadi sumber penularan. Berdasarkan penyelidikan epidemiologi saat ini, masa inkubasinya adalah 1 sampai 14 hari, kebanyakan 3 sampai 7 hari.Manifestasi utamanya meliputi demam, kelelahan, dan batuk kering.Hidung tersumbat, pilek, sakit tenggorokan, mialgia, dan diare ditemukan pada beberapa kasus.
REAGEN
Kaset uji mengandung partikel protein Nukleokapsid anti-SARS-CoV-2 dan protein Nukleokapsid anti-SARS-CoV-2 yang dilapisi membran.
TINDAKAN PENCEGAHAN
Harap baca semua informasi dalam sisipan paket ini sebelum melakukan tes.
1. Hanya untuk penggunaan diagnostik in vitro profesional.Jangan gunakan setelah tanggal kedaluwarsa.
2. Tes harus tetap berada dalam kantong tertutup sampai siap digunakan.
3.Semua spesimen harus dianggap berpotensi berbahaya dan ditangani dengan cara yang sama seperti agen infeksi.
4. Tes bekas harus dibuang sesuai dengan peraturan setempat.
5.Hindari penggunaan sampel berdarah.
6. Kenakan sarung tangan saat menyerahkan sampel, hindari menyentuh membran reagen dan sampel dengan baik.
PENYIMPANAN DAN STABILITAS
Masa berlakunya adalah 18 bulan jika produk ini disimpan di lingkungan
2-30℃.Tes stabil melalui tanggal kedaluwarsa yang tercetak pada kantong tertutup.Tes harus tetap berada di dalam kantong tertutup sampai digunakan.JANGAN DIBEKUKAN.Jangan gunakan melebihi tanggal kedaluwarsa.
PENGUMPULAN DAN PERSIAPAN SPESIMEN
1. Pengumpulan sekret tenggorokan: Masukkan usap steril ke dalam tenggorokan seluruhnya dari mulut, berpusat pada dinding tenggorokan dan area amandel langit-langit yang memerah, usap amandel faring bilateral dan dinding faring posterior dengan gerakan sedang.
paksa, hindari menyentuh lidah dan keluarkan kapasnya.
2. Segera proses sampel dengan larutan ekstraksi sampel yang disediakan dalam kit setelah sampel dikumpulkan.Apabila tidak dapat segera diproses, sebaiknya sampel disimpan dalam tabung plastik kering, steril, dan tertutup rapat.Dapat disimpan pada suhu 2-8℃ selama 8 jam, dan dapat disimpan dalam waktu lama pada suhu -70℃.
3. Sampel yang sangat terkontaminasi dengan sisa makanan di mulut tidak dapat digunakan untuk pengujian produk ini.Sampel yang dikumpulkan dari penyeka yang terlalu kental atau menggumpal tidak disarankan untuk pengujian produk ini.Jika penyeka terkontaminasi dengan darah dalam jumlah besar, tidak disarankan untuk pengujian.Tidak disarankan menggunakan sampel yang diproses dengan larutan ekstraksi sampel yang tidak disediakan dalam kit ini untuk pengujian produk ini.
KOMPONEN KIT
Bahan menyediakan
| Kaset uji | Reagen Ekstraksi | Tabung ekstraksi | |
| Penyeka Steril | Sisipan Paket | Stasiun Kerja |
Bahan diperlukan tetapi tidak disediakan
| pengatur waktu | Untuk penggunaan waktu. |
| Kemasan |
Spesifikasi25
tes/paket50
tes/paket100
tes/paketReagen Ekstraksi Sampel25 tes/paket50 tes/paket100 tes/paketEkstraksi sampel
tabung≥25 tes/paket≥50 tes/paket≥100 tes/paketInstruksiLihat ke
paketRujuk ke
paketRujuk ke
kemasan
PETUNJUK PENGGUNAAN
Biarkan pengujian, spesimen, buffer ekstraksi seimbang dengan suhu kamar (15-30℃) sebelum pengujian.
1.Keluarkan kaset tes dari kantong foil yang tersegel dan gunakan dalam waktu 15 menit.Hasil terbaik akan diperoleh jika pengujian dilakukan segera setelah kantong foil dibuka.
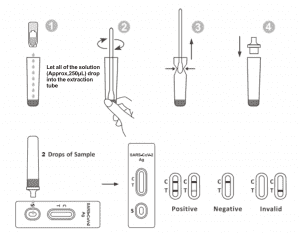
2. Letakkan Tabung Ekstraksi di tempat kerja. Pegang botol reagen ekstraksi secara terbalik secara vertikal. Peras botol dan biarkan semua larutan (Sekitar 250μL) jatuh ke dalam tabung ekstraksi dengan bebas tanpa menyentuh tepi tabung ke tempat Ekstraksi. Tabung.
3. Masukkan spesimen usap ke dalam Tabung Ekstraksi. Putar usap selama kurang lebih 10 detik sambil menekan kepala pada bagian dalam tabung untuk melepaskan antigen yang ada di dalam usap.
4.Keluarkan kapas sambil menekan kepala kapas ke bagian dalam Tabung Ekstraksi saat Anda mengeluarkannya untuk mengeluarkan cairan sebanyak mungkin dari kapas tersebut. Buang kapas tersebut sesuai dengan protokol pembuangan limbah biohazard Anda.
5.Pasang ujung penetes di atas tabung ekstraksi. Letakkan kaset tes pada permukaan yang bersih dan rata.
6.Tambahkan 2 tetes larutan (kira-kira 65μL) ke dalam sampel dengan baik dan kemudian mulai pengatur waktu. Baca hasil yang ditampilkan dalam 20-30 menit, dan hasil yang dibaca setelah 30 menit tidak valid.
INTERPRETASI HASIL
| NEGATIF HASIL: |
Satu garis berwarna muncul di wilayah garis kontrol (C).Tidak ada garis yang muncul di wilayah pengujian (T). Hasil negatif menunjukkan bahwa antigen SARS-CoV-2 tidak ada dalam spesimen, atau berada di bawah tingkat yang terdeteksi pada pengujian.
POSITIFHASIL:
Dua garis muncul. Satu garis berwarna harus berada di wilayah kontrol (C) dan garis berwarna lainnya harus berada di wilayah pengujian (T). Hasil positif menunjukkan bahwa SARS-CoV-2 terdeteksi pada spesimen.
HASIL TIDAK VALID:
Garis kontrol gagal muncul. Volume spesimen yang tidak memadai atau teknik prosedur yang salah kemungkinan besar menjadi penyebab kegagalan garis kontrol.Tinjau prosedurnya dan ulangi tes dengan tes baru.Jika masalah terus berlanjut, segera hentikan penggunaan alat tes dan hubungi distributor setempat Anda.
CATATAN:
Intensitas warna pada wilayah garis uji (T) akan bervariasi tergantung pada konsentrasi Antigen SARS-CoV-2 yang ada dalam spesimen.Oleh karena itu, setiap bayangan warna di wilayah garis uji (T) harus dianggap positif.
KONTROL KUALITAS
- Kontrol prosedural disertakan dalam tes.Garis berwarna yang muncul di wilayah kontrol (C) dianggap sebagai kontrol prosedural internal. Ini memastikan penyerapan membran yang memadai.
- Standar kontrol tidak disertakan dengan kit ini;namun, direkomendasikan agar kontrol positif dan negatif diuji sebagai praktik laboratorium yang baik untuk memastikan prosedur pengujian dan memverifikasi kinerja pengujian yang tepat.
BATASANUJI
- ItuKaset Tes Cepat Antigen SARS-CoV-2hanya untuk penggunaan diagnostik in vitro profesional. Tes ini sebaiknya digunakan untuk mendeteksi Antigen SARS-CoV-2 pada Swab Oropharyngeal. Baik nilai kuantitatif maupun laju peningkatan konsentrasi SARS-CoV-2 tidak dapat ditentukan dengan kualitatif ini tes.
- Keakuratan pengujian bergantung pada kualitas sampel usap. Negatif palsu dapat terjadi akibat penyimpanan pengumpulan sampel yang tidak tepat.
- Kaset Tes Cepat Antigen SARS-CoV-2 hanya akan menunjukkan keberadaan SARS-CoV-2 dalam spesimen dari strain virus corona SARS-CoV-2 yang dapat hidup dan tidak dapat hidup.
- Seperti semua tes diagnostik, semua hasil harus diinterpretasikan bersama dengan informasi klinis lain yang tersedia bagi dokter.
- Hasil negatif yang diperoleh dari kit ini harus dikonfirmasi dengan PCR. Hasil negatif dapat diperoleh jika konsentrasi SARS-CoV-2 yang ada pada usap tidak mencukupi atau berada di bawah tingkat deteksi tes.
- Darah atau lendir berlebih pada spesimen usap dapat mengganggu kinerja dan dapat memberikan hasil positif palsu.
- Hasil positif untuk SARS-CoV-2 tidak menghalangi terjadinya koinfeksi dengan patogen lain.Oleh karena itu, kemungkinan infeksi bakteri yang mendasarinya harus dipertimbangkan.
- Hasil negatif tidak menutup kemungkinan adanya infeksi SARS-CoV-2, terutama pada mereka yang pernah melakukan kontak dengan virus tersebut.Tes tindak lanjut dengan diagnostik molekuler harus dipertimbangkan untuk menyingkirkan kemungkinan infeksi pada orang-orang ini.
- Hasil positif mungkin disebabkan oleh infeksi jenis virus corona non-SARS-CoV-2, seperti virus corona HKU1,NL63,OC43, atau 229E.
- Hasil tes antigen tidak boleh digunakan sebagai satu-satunya dasar untuk mendiagnosis atau mengecualikan infeksi SARS-CoV-2 atau untuk menginformasikan status infeksi.
- Reagen ekstraksi mempunyai kemampuan membunuh virus, namun tidak dapat menonaktifkan 100% virus. Cara menonaktifkan virus dapat mengacu pada: cara apa yang direkomendasikan oleh WHO/CDC, atau dapat ditangani sesuai peraturan setempat.
KARAKTERISTIK KINERJA
KepekaanDanKekhususan
Kaset Tes Cepat Antigen SARS-CoV-2 telah dievaluasi dengan spesimen yang diperoleh dari pasien. PCR digunakan sebagai metode referensi untuk Kaset Tes Cepat Antigen SARS-CoV-2. Spesimen dianggap positif jika PCR menunjukkan hasil positif.
| metode | RT-PCR | Hasil Jumlah | ||
| Kaset Tes Cepat Antigen SARS-CoV-2 | Hasil | Positif | Negatif | |
| Positif | 38 | 3 | 41 | |
| Negatif | 2 | 360 | 362 | |
| Hasil Jumlah | 40 | 363 | 403 | |
Sensitivitas Relatif :95,0%(95%CI*:83,1%-99,4%)
Kekhususan Relatif:99,2%(95%CI*:97,6%-99,8%)
*Interval Keyakinan
Batas Deteksi
Ketika konten virus lebih besar dari 400TCID50/ml, tingkat deteksi positif lebih besar dari 95%.Ketika konten virus kurang dari 200TCID50/ml, tingkat deteksi positif kurang dari 95%, sehingga batas deteksi minimum produk ini adalah 400TCID50/ml.
Presisi
Tiga batch reagen berturut-turut diuji presisinya.Kumpulan reagen yang berbeda digunakan untuk menguji sampel negatif yang sama 10 kali berturut-turut, dan hasilnya semuanya negatif.Kumpulan reagen yang berbeda digunakan untuk menguji sampel positif yang sama sebanyak 10 kali berturut-turut, dan hasilnya semuanya positif.
efek KAIT
Ketika kandungan virus dalam sampel yang akan diuji mencapai 4.0*105TCID50/ml, hasil tes masih belum menunjukkan efek HOOK.
Reaktivitas Silang
Reaktivitas silang Kit dievaluasi.Hasilnya menunjukkan tidak ada reaktivitas silang dengan spesimen berikut.
| Nama | Konsentrasi |
| HCOV-HKU1 | 105TCID50/ml |
| Stafilokokus aureus | 106TCID50/ml |
| Streptokokus grup A | 106TCID50/ml |
| virus campak | 105TCID50/ml |
| virus gondongan | 105TCID50/ml |
| Adenovirus tipe 3 | 105TCID50/ml |
| Pneumonia mikoplasma | 106TCID50/ml |
| Paraimfluenzavirus, tipe 2 | 105TCID50/ml |
| virus metapneumo manusia | 105TCID50/ml |
| Virus corona manusia OC43 | 105TCID50/ml |
| Virus corona manusia 229E | 105TCID50/ml |
| Parapertusis Bordetella | 106TCID50/ml |
| STRAIN Influenza B Victoria | 105TCID50/ml |
| Influenza B YSTRAIN | 105TCID50/ml |
| Influenza A H1N1 2009 | 105TCID50/ml |
| Influenza A H3N2 | 105TCID50/ml |
| H7N9 | 105TCID50/ml |
| H5N1 | 105TCID50/ml |
| virus Epstein-Barr | 105TCID50/ml |
| Enterovirus CA16 | 105TCID50/ml |
| virus badak | 105TCID50/ml |
| Virus sinsitium saluran pernapasan | 105TCID50/ml |
| Streptococcus pneumoniae-ae | 106TCID50/ml |
| Candida albicans | 106TCID50/ml |
| Klamidia pneumoniae | 106TCID50/ml |
| Bordetella pertusis | 106TCID50/ml |
| Pneumocystis jiroveci | 106TCID50/ml |
| Mycobacterium tuberkulosis | 106TCID50/ml |
| Legionella pneumophila | 106TCID50/ml |
Imengganggu Zat
Hasil pengujian tidak boleh dicampuri dengan zat pada konsentrasi sebagai berikut:
| Mengganggu zat | Kesimpulan | Mengganggu substansi | Kesimpulan |
| Seluruh darah | 4% | Gel Benzoin Senyawa | 1,5mg/ml |
| Ibuprofen | 1mg/ml | Kromolin glikat | 15% |
| tetrasiklin | 3ug/ml | kloramfenikol | 3ug/ml |
| musin | 0,5% | mupirosin | 10 mg/ml |
| Eritromisin | 3ug/ml | Oseltamivir | 5mg/ml |
| Tobramisin | 5% | Tetes Hidung Naphazoline Hydrochlo-ride | 15% |
| menthol | 15% | Semprotan flutikason propionat | 15% |
| Afrin | 15% | Deoksiepinefrin hidroklorida | 15% |
IBIBLIOGRAFI
1.Weiss SR,Leibowitz JZ.Patogenesis virus corona.Adv Virus Res 2011;81:85-164
2.Cui J,Li F,Shi ZL.Asal usul dan evolusi virus corona patogen.Nat Rev Microbiol 2019;17:181-192.
3.Su S,Wong G,Shi W, dkk.Epidemiologi, rekombinasi genetik, dan patogenesis virus corona.TrenMikrobiol 2016;24:490-502.