COVID-19 IgG/IgM Schnelltestkassett
Kuerz Beschreiwung:
D'COVID-19 IgG/IgM Schnelltestkassett ass e Lateral-Flow-Immunoassay, dee fir d'qualitativ Noweis vun IgG- an IgM-Antikörper géint de SARS-CoV-2-Virus a Vollblut-, Serum- oder Plasmaprouwen vu Persounen entwéckelt gouf, bei deenen hire Gesondheetsspezialist verdächtegt huet, eng COVID-19-Infektioun ze hunn.
Den CO VID-19 IgG/IgM Schnelltest ass eng Hëllefsmëttel bei der Diagnos vu Patienten mat Verdacht op SARS-CoV-2 Infektioun a Verbindung mat der klinescher Presentatioun an de Resultater vun aneren Labortester. Et gëtt proposéiert als zousätzlechen Testindikator fir Verdachtsfäll mat negativen Nukleinsäuretest fir nei Coronavirus ze benotzen oder a Verbindung mat engem Nukleinsäuretest a Verdachtsfäll ze benotzen. Resultater vun Antikörpertester sollten net als eenzeg Basis benotzt ginn fir eng SARS-CoV-2 Infektioun ze diagnostizéieren oder auszeschléissen oder fir den Infektiounsstatus ze bestëmmen.
Negativ Resultater schléissen eng SARS-CoV-2 Infektioun net aus, besonnesch bei deenen, déi a Kontakt mat bekannt infizéierte Persoune waren oder a Gebidder mat enger héijer Prävalenz vun aktiver Infektioun. Nofolgte Tester mat engem molekulare Diagnostikinstrument sollten a Betruecht gezunn ginn, fir eng Infektioun bei dëse Persounen auszeschléissen.
Positiv Resultater kënnen op eng vergaangen oder aktuell Infektioun mat net-SARS-CoV-2 Coronavirus-Stämme zréckzeféieren sinn.
Den Test ass geduecht fir a klineschen Laboratoiren oder vu Gesondheetsfachleit um Point-of-Care benotzt ze ginn, net fir den Heemgebrauch. Den Test soll net fir den Screening vu gespendetem Blutt benotzt ginn.
Nëmme fir professionell an in-vitro-diagnostesch Benotzung.
Nëmme fir professionell an in-vitro-diagnostesch Benotzung.
GEWICHTEG BENOTZUNG
DenCOVID-19 IgG/IgM Schnelltestkassettass e lateral-flow-Immunoassay, dee fir d'qualitativ Noweis vun IgG- an IgM-Antikörper géint de SARS-CoV-2-Virus a Vollblut-, Serum- oder Plasmaprouwen vu Persounen entwéckelt gouf, bei deenen hire Gesondheetsspezialist verdächtegt huet, eng COVID-19-Infektioun ze hunn.
Den CO VID-19 IgG/IgM Schnelltest ass eng Hëllefsmëttel bei der Diagnos vu Patienten mat Verdacht op SARS-CoV-2 Infektioun a Verbindung mat der klinescher Presentatioun an de Resultater vun aneren Labortester. Et gëtt proposéiert als zousätzlechen Testindikator fir Verdachtsfäll mat negativen Nukleinsäuretest fir nei Coronavirus ze benotzen oder a Verbindung mat engem Nukleinsäuretest a Verdachtsfäll ze benotzen. Resultater vun Antikörpertester sollten net als eenzeg Basis benotzt ginn fir eng SARS-CoV-2 Infektioun ze diagnostizéieren oder auszeschléissen oder fir den Infektiounsstatus ze bestëmmen.
Negativ Resultater schléissen eng SARS-CoV-2 Infektioun net aus, besonnesch bei deenen, déi a Kontakt mat bekannt infizéierte Persoune waren oder a Gebidder mat enger héijer Prävalenz vun aktiver Infektioun. Nofolgte Tester mat engem molekulare Diagnostikinstrument sollten a Betruecht gezunn ginn, fir eng Infektioun bei dëse Persounen auszeschléissen.
Positiv Resultater kënnen op eng vergaangen oder aktuell Infektioun mat net-SARS-CoV-2 Coronavirus-Stämme zréckzeféieren sinn.
Den Test ass geduecht fir a klineschen Laboratoiren oder vu Gesondheetsfachleit um Point-of-Care benotzt ze ginn, net fir den Heemgebrauch. Den Test soll net fir den Screening vu gespendetem Blutt benotzt ginn.
ZESUMMEFAASSUNG
Déi nei Coronaviren gehéieren zu der Gattung p.COVID 19ass eng akut respiratoresch Infektiounskrankheet. D'Leit si generell ufälleg dofir. Aktuell sinn d'Patienten, déi mam neie Coronavirus infizéiert sinn, déi Haaptquell vun der Infektioun; asymptomatesch infizéiert Persoune kënnen och eng Infektiounsquell sinn. Baséierend op der aktueller epidemiologescher Ënnersichung ass d'Inkubatiounszäit 1 bis 14 Deeg, meeschtens 3 bis 7 Deeg. Déi Haaptmanifestatioune sinn Féiwer, Middegkeet an dréchenen Houscht. Verstoppte Nues, laafend Nues, Halswéi, Muskelschmerzen an Duerchfall ginn a wéinege Fäll festgestallt.
Wann de SARS-CoV2-Virus en Organismus infizéiert, ass d'RNA, dat genetescht Material vum Virus, den éischte Marker, deen nogewise ka ginn. De Profil vun der viraler Belaaschtung vu SARS-CoV-2 ass ähnlech wéi dee vun der Gripp, deen säi Maximum ongeféier zum Zäitpunkt vum Ufank vun de Symptomer erreecht an dann ufänkt ofzehuelen. Mat der Entwécklung vum Krankheetsverlaf no der Infektioun produzéiert den Immunsystem vum Mënsch Antikörper, dorënner IgM den fréien Antikörper, deen de Kierper no der Infektioun produzéiert, wat op déi akut Phas vun der Infektioun hiweist. IgG-Antikörper géint SARS-CoV2 ginn spéider no der Infektioun nogewise. Positiv Resultater fir souwuel IgG wéi och IgM kéinten no der Infektioun optrieden a kënnen en Hiwäis op eng akut oder rezent Infektioun sinn. IgG weist déi Rekonvaleszenzphase vun der Infektioun oder eng Geschicht vun Infektiounen an der Vergaangenheet un.
Wéi och ëmmer, souwuel IgM wéi och IgG hunn eng Fënsterperiod vun der Virusinfektioun bis zur Antikörperproduktioun, IgM erschéngt bal no dem Ufank vun der Krankheet e puer Deeg, sou datt hir Detektioun dacks hannert der Detektioun vun Nukleinsäuren hänke bleift a manner empfindlech ass wéi d'Detektioun vun Nukleinsäuren. A Fäll wou Nukleinsäure-Amplifikatiounstester negativ sinn an et e staarken epidemiologesche Lien mat ... gëtt.COVID 19Infektioun, kéinten gepaarte Serumprouwen (an der akuter a Rekonvaleszenzphase) d'Diagnos ënnerstëtzen.
PRINZIP
D'COVID-19 IgG/IgM Schnelltestkassett (WB/S/P) ass e qualitativen Immunoassay op Basis vu Membranstreifen fir den Noweis vun Antikörper (IgG an IgM) géint den neie Coronavirus am mënschleche Vollblutt/Serum/Plasma. D'Testkassett besteet aus:1) e bordeauxrout Koijugat-Pad mat rekombinante Hülle-Antigenen aus dem neie Coronavirus, déi mat Kolloidgold koijugéiert sinn (nei Coronavirus-Coronavirus ...两(IgG- an IgM-Linnen), 2) en Nitrocellulosemembranstreifen mat zwou Testlinnen (IgG- an IgM-Linnen) an enger Kontrolllinn (C-Linn). D'IgM-Linn ass virbeschichtet mat dem Maus-Anti-Mënsch-IgM-Antikörper, d'IgG-Linn ass mat engem Maus-Anti-Mënsch-IgG-Antikörper beschichtet, wann eng ausreechend Quantitéit vun enger leschter Prouf an de Prouflach vun der Testkassett geliwwert gëtt. D'Prouf migréiert duerch Kapillarwierkung iwwer d'Kassett. IgM Anti-Nei-Coronavirus, wann an der Prouf präsent, bindt sech un d'Nei-Coronavirus-Konjugater. Den Immunkomplex gëtt dann vum Reagens agefaangen, deen op der IgM-Band virbeschichtet ass, wouduerch eng bordeauxrout IgM-Linn entsteet, wat op e positivt Testergebnis fir den Nei-Coronavirus-IgG hiweist. Den IgG Anti-Nei-Coronavirus, deen an der Prouf präsent ass, bindt sech un d'Nei-Coronavirus-Konjugater. Den Immunkomplex gëtt dann vum Reagens agefaangen, deen op der IgG-Linn beschichtet ass, wouduerch eng bordeauxrout IgG-Linn entsteet, wat op e positivt Testergebnis fir den Nei-Coronavirus-IgG hiweist. D'Feele vun T-Linnen (IgG an IgM) weist op eng
negativt Resultat. Fir als prozedural Kontroll ze déngen, erschéngt ëmmer eng faarweg Linn am Kontrolllinnberäich, déi beweist, datt de richtege Volumen vun der Probe bäigefüügt gouf an d'Membranofwicklung geschitt ass.
WARNUNGEN A VIRSIICHTSMOOSNAMEN
- Nëmme fir in-vitro-diagnostesch Benotzung.
- Fir Gesondheetsspezialisten a Fachleit op Point-of-Care-Plazen.
•Net nom Verfallsdatum benotzen.
- Liest w.e.g. all Informatiounen an dëser Broschür ier Dir den Test duerchféiert. • D'Testkassett soll bis zur Benotzung an der zouener Täsch bleiwen.
•All Prouwe solle als potenziell geféierlech ugesi ginn a solle wéi en infektiéisen Agent behandelt ginn.
•Déi benotzt Testkassett soll geméiss de federalen, staatlechen a lokalen Reglementer entsuergt ginn.
ZESUMMESETZUNG
Den Test enthält e Membranstreifen, deen mat Maus-Anti-Mënsch-IgM-Antikörper a Maus-Anti-Mënsch-IgG-Antikörper beschichtet ass.
Testlinn, an e Faarfpad, deen kolloidalt Gold gekoppelt mat engem rekombinanten Antigen vum neie Coronavirus enthält. D'Quantitéit vun den Tester gouf op der Etikettéierung gedréckt.
Materialien déi geliwwert ginn
- Testkassett • Packungsbeilage
- Puffer • Drëps
- Lancet
Materialien déi néideg sinn, awer net geliwwert ginn
•Behälter fir d'Proufensammlung • Timer
LAGERUNG A STABILITÉIT
•Wéi verpackt an der zouener Täsch bei der Temperatur (4-30″ oder 40-86°F) lageren. De Kit ass bannent dem Verfallsdatum, deen op der Etikett gedréckt ass, stabil.
• Nodeems d'Täsch opgemaach gouf, soll d'Täsch bannent enger Stonn benotzt ginn. Längeren Kontakt mat waarmer a fiichter Ëmwelt féiert zu enger Verschlechterung vum Produkt.
•D'LOT an den Verfallsdatum waren op der Etikettéierung gedréckt.
•Den Test kann benotzt ginn fir Vollblut-/Serum-/Plasmaproben ze testen.
• Fir Vollblut-, Serum- oder Plasmaproben no reegelméissege klineschen Laborprozeduren ze sammelen.
•Trennt Serum oder Plasma sou séier wéi méiglech vum Blutt fir Hämolyse ze vermeiden. Benotzt nëmme kloer, net-hämolyséiert Proben.
•Prouwe bei 2-8 °C (36-46 °T) späicheren, wa se net direkt getest ginn. Prouwe bis zu 7 Deeg bei 2-8 °C späicheren. D'Prouwe solle bei -20 °C (-4 °F) agefruer ginn, fir eng méi laang Lagerung. Vollblutprouwe net afréieren.、
•Vermeit multiple Gefrier- an Optau-Zyklen. Virum Test sollten déi gefruer Proben lues op Raumtemperatur bruecht ginn a virsiichteg vermëscht ginn.
Proben, déi siichtbar partikelfërmeg Matière enthalen, solle virum Test duerch Zentrifugatioun gekläert ginn.
•Benotzt keng Proben, déi eng grouss Lipämie, eng grouss Hämolyse oder eng Trübung weisen, fir Stéierungen an der Interpretatioun vun de Resultater ze vermeiden.
TESTPROCEDUR
Loosst den Testapparat an d'Prouwe virum Test op d'Temperatur (15-30 °C oder 59-86 °T) gläichméisseg reagéieren.
- Huelt d'Testkassett aus der zouener Täsch eraus.
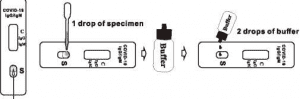
- Halt den Drëpsen vertikal a gitt 1 Drëps (ongeféier 10 µl) vun der Prouf an den ieweschten Deel vum Proufschacht (S) a passt op, datt keng Loftblosen do sinn. Fir eng besser Präzisioun, transferéiert d'Prouf mat enger Pipett, déi fäeg ass, 10 µl Volumen ze liwweren. Kuckt d'Illustratioun hei ënnendrënner.
- Dann, direkt 2 Drëpsen (ongeféier 70 µl) Puffer an de Prouflach (S) bäiginn.
- Start den Timer.
- bis faarweg Linnen erscheinen. Interpretéiert d'Testergebnisse no 15 Minutten. Liest d'Resultater net no 20 Minutten.
Beräich fir Prouf
(D'Bild ass nëmme fir Referenz, kuckt w.e.g. op den Objet.)
INTERPRETATIOUN VUN DE RESULTATER
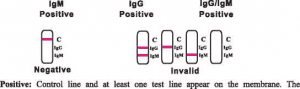
Antikörper. D'Erscheinung vun enger IgM-Testlinn weist d'Präsenz vun IgM-Antikörper, déi spezifesch fir den neie Coronavirus sinn, un. A wann souwuel eng IgG- wéi och eng IgM-Linn erschéngen, weist dat d'Präsenz vun IgG- an IgM-Antikörper, déi spezifesch fir den neie Coronavirus sinn.
Negativ:Eng faarweg Linn erschéngt an der Kontrollregioun (C), keng offensichtlech faarweg Linn erschéngt an der Testlinnregioun.
Ongülteg:D'Kontrolllinn erschéngt net. Net genuch Proufvolumen oder falsch Prozedurtechnike sinn déi warscheinlechst Ursaachen fir e Feeler vun der Kontrolllinn. Iwwerpréift d'Prozedur a widderhuelt den Test mat enger neier Testkassett. Wann de Problem bestoe bleift, stoppt direkt d'Benotzung vum Testkit a kontaktéiert Äre lokale Distributeur.
QUALITÉITSKONTROLL
Eng prozedural Kontroll ass am Test abegraff. Eng faarweg Linn, déi an der Kontrollregioun (C) erschéngt, gëllt als intern prozedural Kontroll. Si bestätegt e genuch Probevolumen, eng adäquat Membranabsorptioun an eng korrekt prozedural Technik. Kontrollstandarde ginn net mat dësem Kit geliwwert. Et ass awer recommandéiert, positiv an negativ Kontrollen als gutt Laborpraxis ze testen, fir d'Testprozedur ze bestätegen an déi richteg Testleistung ze verifizéieren.
ASCHRÄNKUNGEN
• D'COVID-19 IgG/IgM Schnelltestkassett (WB/S/P) ass limitéiert fir eng qualitativ Analyse ze liwweren
Detektioun. D'Intensitéit vun der Testlinn korreléiert net onbedéngt mat der Konzentratioun vum Antikörper am Blutt. D'Resultater vun dësem Test sinn nëmmen als Hëllefsmëttel bei der Diagnos geduecht. All Dokter muss d'Resultater a Verbindung mat der Geschicht vum Patient, de kierperleche Befunde an aneren diagnostesche Prozeduren interpretéieren.
•En negativt Testergebnis weist drop hin, datt Antikörper géint den neie Coronavirus entweder keng sinn oder a Konzentratioune sinn, déi mam Test net nogewise kënne ginn.
Leeschtungseigenschaften
Genauegkeet
Zesummefassungsdaten vum CO VID-19 IgG/IgM Schnelltest wéi hei ënnendrënner
Wat den IgG-Test ugeet, hu mir déi positiv Rate vun den 82 Patienten während der Rekonvaleszenzperiod gezielt.
COVID-19 IgG:
| COVID-19 IgG | Zuel vun de Patienten während der Rekonvaleszenzperiod | Total |
| Positiv | 80 | 80 |
| Negativ | 2 | 2 |
| Total | 82 | 82 |
D'Resultater hunn eng Sensibilitéit vun 97,56% erginn.
Wat den IgM-Test ugeet, de Verglach vum Resultat mam RT-PCR.
COVID-19 IgM:
| COVID-19 IgM | RT-PCR | Total | |
| Positiv | Negativ | ||
| Positiv | 70 | 2 | 72 |
| Negativ | 9 | 84 | 93 |
| Total | 79 | 86 | 165 |
E statistesche Verglach gouf tëscht de Resultater gemaach, wat eng Sensibilitéit vun 88,61%, eng Spezifitéit vun 97,67% an eng Genauegkeet vun 93,33% erginn huet.
Kräizreaktivitéit an Interferenz
1. Aner heefeg Ursaache vun infektiösen Krankheeten goufen op Kräizreaktivitéit mam Test evaluéiert. E puer positiv Prouwe vun aneren heefegen infektiösen Krankheeten goufen an d'Prouwe vum neie Coronavirus positiv an negativ bäigefüügt a separat getest. Et gouf keng Kräizreaktivitéit mat Prouwe vu Patienten observéiert, déi mat HIV, HA^ HBsAg, HCV TP, HTIA^ CMV FLUA, FLUB, RSy MP, CP, HPIVs infizéiert waren.
2. Potenziell kräizreaktiv endogen Substanzen, dorënner üblech Serumkomponenten, wéi Lipiden, Hämoglobin a Bilirubin, goufen a héije Konzentratioune mat positiven a negativen Proben vum neie Coronavirus agefouert an separat getest.
Et gouf keng Kräizreaktivitéit oder Interferenz mam Apparat observéiert.
| Analyten | Kegel. | Exemplare | |
| Positiv | Negativ | ||
| Albumin | 20 mg/ml | + | |
| Bilirubin | 20p,g/ml | + | |
| Hämoglobin | 15 mg/ml | + | |
| Glukos | 20 mg/ml | + | |
| Harnsäure | 200 µm g/ml | + | |
| Lipiden | 20 mg/ml | + | |
3. Aner üblech biologesch Analyten goufen an déi positiv an negativ Prouwe vum neie Coronavirus agefouert a separat getest. Et gouf keng bedeitend Stéierung bei de Niveauen, déi an der Tabell hei ënnendrënner opgezielt sinn, observéiert.
| Analyten | Konzentratioun (gg/ ml) | Exemplare | |
| Positiv | Negativ | ||
| Acetoessigsäure | 200 | + | |
| Acetylsalicylsäure | 200 | + | |
| Benzoylecgonin | 100 | + | |
| Koffein | 200 | + | |
| EDTA | 800 | + | |
| Ethanol | 1,0% | + | |
| Gentisinsäure | 200 | + | |
| p-Hydroxybutyrat | 20.000 | + | |
| Methanol | 10,0% | + | |
| Phenothiazin | 200 | + | |
| Phenylpropanolamin | 200 | + | |
| Salicylsäure | 200 | + | |
| Paracetamol | 200 | + | |
Reproduzéierbarkeet
Reproduzéierbarkeetsstudien goufen fir den Novel Coronavirus IgG/IgM Rapid Test an dräi Dokterpraxislaboratoiren (POL) duerchgefouert. Siechzeg (60) klinesch Serumprouwen, 20 negativ, 20 Grenzpositiv an 20 positiv, goufen an dëser Studie benotzt. All Prouf gouf dräi Deeg laang an all POL dräimol getest. D'Iwwereneestëmmung tëscht den Assays war 100%. D'Iwwereneestëmmung tëscht de verschiddene Laboratoiren war 100%.