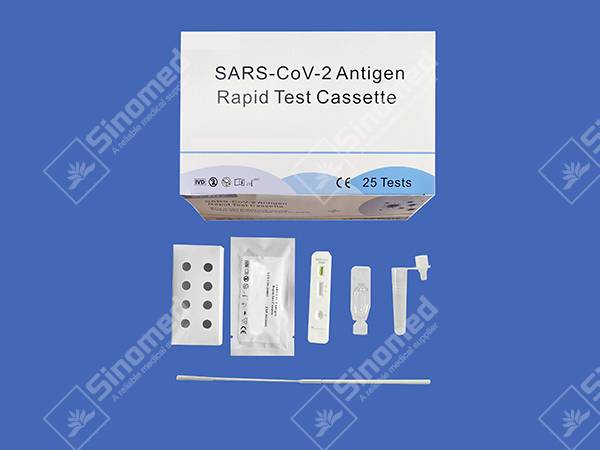
ตลับทดสอบแบบรวดเร็วสำหรับแอนติเจน SARS-CoV-2
คำอธิบายสั้น ๆ :
ชุดทดสอบแบบเร่งด่วนแอนติเจน SARS-CoV-2 เป็นชุดทดสอบทางโครมาโตกราฟีแบบรวดเร็วสำหรับการตรวจหาแอนติเจน SARS-CoV-2 เชิงคุณภาพในสำลีจากช่องปากและคอหอยของมนุษย์ การระบุนี้ใช้แอนติบอดีโมโนโคลนอลที่จำเพาะต่อโปรตีนนิวคลีโอแคปซิด (N) ของ SARS-CoV-2 โดยมีจุดประสงค์เพื่อช่วยในการวินิจฉัยแยกโรคติดเชื้อ COVID-19 อย่างรวดเร็ว
การใช้งานที่ตั้งใจ
การตลับทดสอบแบบรวดเร็วสำหรับแอนติเจน SARS-CoV-2เป็นการทดสอบภูมิคุ้มกันแบบโครมาโทกราฟีอย่างรวดเร็วสำหรับการตรวจหาแอนติเจน SARS-CoV-2 เชิงคุณภาพในสำลีจากช่องปากและคอหอยของมนุษย์ การระบุนี้ใช้แอนติบอดีโมโนโคลนอลที่จำเพาะต่อโปรตีนนิวคลีโอแคปซิด (N) ของ SARS-CoV-2 มีจุดประสงค์เพื่อช่วยในการวินิจฉัยแยกโรคอย่างรวดเร็วโควิด 19การติดเชื้อ.
ข้อมูลจำเพาะของแพ็คเกจ
25 ทดสอบ/แพ็ค, 50 ทดสอบ/แพ็ค, 100 ทดสอบ/แพ็ค
การแนะนำ
ไวรัสโคโรนาสายพันธุ์ใหม่จัดอยู่ในสกุล βโควิด 19เป็นโรคติดเชื้อทางเดินหายใจเฉียบพลัน โดยทั่วไปแล้วผู้คนมีความเสี่ยงต่อการติดเชื้อ ปัจจุบัน ผู้ป่วยที่ติดเชื้อไวรัสโคโรนาสายพันธุ์ใหม่เป็นแหล่งแพร่เชื้อหลัก ผู้ติดเชื้อที่ไม่มีอาการก็สามารถแพร่เชื้อได้เช่นกัน จากการตรวจสอบทางระบาดวิทยาในปัจจุบัน ระยะฟักตัวอยู่ที่ 1 ถึง 14 วัน ส่วนใหญ่ 3 ถึง 7 วัน อาการหลัก ได้แก่ มีไข้ อ่อนเพลีย และไอแห้ง ในบางกรณีอาจมีอาการคัดจมูก น้ำมูกไหล เจ็บคอ ปวดกล้ามเนื้อ และท้องเสีย
สารเคมี
ตลับทดสอบประกอบด้วยอนุภาคโปรตีนนิวคลีโอแคปซิดต่อต้าน SARS-CoV-2 และโปรตีนนิวคลีโอแคปซิดต่อต้าน SARS-CoV-2 ที่เคลือบอยู่บนเมมเบรน
ข้อควรระวัง
โปรดอ่านข้อมูลทั้งหมดในเอกสารแนบนี้ก่อนดำเนินการทดสอบ
1. สำหรับการวินิจฉัยในหลอดทดลองโดยผู้เชี่ยวชาญเท่านั้น ห้ามใช้หลังวันหมดอายุ
2.ควรเก็บการทดสอบไว้ในซองที่ปิดสนิทจนกว่าจะพร้อมใช้งาน
3.ตัวอย่างทั้งหมดควรได้รับการพิจารณาว่ามีความเสี่ยงและควรจัดการในลักษณะเดียวกับที่เป็นสารก่อการติดเชื้อ
4.ควรทิ้งการทดสอบที่ใช้แล้วตามระเบียบข้อบังคับท้องถิ่น
5.หลีกเลี่ยงการใช้ตัวอย่างที่มีเลือด
6. สวมถุงมือเมื่อหยิบตัวอย่าง หลีกเลี่ยงการสัมผัสเมมเบรนของสารเคมีและช่องเก็บตัวอย่าง
การจัดเก็บและความเสถียร
ระยะเวลาการใช้งานคือ 18 เดือนหากผลิตภัณฑ์นี้ถูกจัดเก็บในสภาพแวดล้อม
2-30℃ การทดสอบจะเสถียรจนถึงวันหมดอายุที่พิมพ์บนซองปิดผนึก การทดสอบจะต้องคงอยู่ในซองปิดผนึกจนกว่าจะใช้งานห้ามแช่แข็งอย่าใช้เกินวันหมดอายุ
การเก็บและเตรียมตัวอย่าง
1.การเก็บตัวอย่างเสมหะจากคอ: สอดสำลีที่ผ่านการฆ่าเชื้อเข้าไปในคอให้หมดจากปาก โดยให้กึ่งกลางอยู่ที่ผนังคอและบริเวณที่มีรอยแดงของต่อมทอนซิลเพดานปาก เช็ดต่อมทอนซิลคอหอยทั้งสองข้างและผนังคอหอยด้านหลังด้วยสำลีปานกลาง
บังคับโดยหลีกเลี่ยงการสัมผัสลิ้นและดึงสำลีออกมา
2. หลังจากเก็บตัวอย่างแล้ว ให้นำตัวอย่างไปสกัดทันทีด้วยสารละลายสกัดที่ให้มาในชุด หากไม่สามารถสกัดได้ทันที ควรเก็บตัวอย่างไว้ในหลอดพลาสติกที่แห้ง ผ่านการฆ่าเชื้อ และปิดผนึกอย่างแน่นหนา สามารถเก็บตัวอย่างไว้ที่อุณหภูมิ 2-8 องศาเซลเซียส ได้นาน 8 ชั่วโมง และเก็บที่อุณหภูมิ -70 องศาเซลเซียส ได้นาน
3. ห้ามใช้ตัวอย่างที่ปนเปื้อนเศษอาหารในช่องปากจำนวนมากในการทดสอบผลิตภัณฑ์นี้ ไม่แนะนำให้ใช้ตัวอย่างที่เก็บจากสำลีที่มีความหนืดหรือเกาะตัวกันมากเกินไปในการทดสอบผลิตภัณฑ์นี้ หากสำลีปนเปื้อนเลือดปริมาณมาก ไม่แนะนำให้ใช้ตัวอย่างที่ผ่านกระบวนการสกัดตัวอย่างที่ไม่มีให้ในชุดอุปกรณ์นี้ในการทดสอบผลิตภัณฑ์นี้
ส่วนประกอบชุดอุปกรณ์
วัสดุที่ให้มา
| ตลับทดสอบ | สารเคมีสกัด | ท่อสกัด | |
| สำลีฆ่าเชื้อ | เอกสารกำกับบรรจุภัณฑ์ | สถานีทำงาน |
วัสดุที่ต้องการแต่ไม่ได้จัดเตรียมให้
| ตัวจับเวลา | สำหรับการจับเวลา |
| บรรจุุภัณฑ์ |
ข้อมูลจำเพาะ25
ทดสอบ/แพ็ค50
ทดสอบ/แพ็ค100
ทดสอบ/แพ็ค สารเคมีสกัดตัวอย่าง 25 การทดสอบ/แพ็ค 50 การทดสอบ/แพ็ค 100 การทดสอบ/แพ็ค การสกัดตัวอย่าง
หลอด≥25 การทดสอบ/แพ็ค≥50 การทดสอบ/แพ็ค≥100 การทดสอบ/แพ็คคำแนะนำดูที่
แพ็คเกจอ้างอิงจาก
แพ็คเกจอ้างอิงจาก
บรรจุุภัณฑ์
วิธีใช้
ปล่อยให้การทดสอบ ตัวอย่าง และบัฟเฟอร์สกัดปรับสมดุลจนถึงอุณหภูมิห้อง (15-30℃) ก่อนทำการทดสอบ
1. นำตลับทดสอบออกจากซองฟอยล์ที่ปิดผนึกและใช้ภายใน 15 นาที จะให้ผลลัพธ์ที่ดีที่สุดหากทำการทดสอบทันทีหลังจากเปิดซองฟอยล์
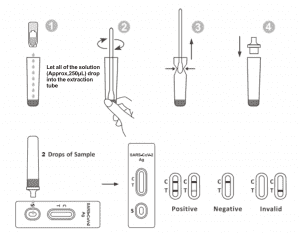
2. วางหลอดสกัดไว้ที่สถานีทำงาน ถือขวดสารเคมีสกัดคว่ำลงในแนวตั้ง บีบขวดและปล่อยให้สารละลายทั้งหมด (ประมาณ 250 μL) หยดลงในหลอดสกัดได้อย่างอิสระ โดยไม่สัมผัสขอบของหลอดกับหลอดสกัด
3. วางตัวอย่างสำลีลงในหลอดสกัด หมุนสำลีประมาณ 10 วินาทีในขณะที่กดส่วนหัวเข้ากับด้านในของหลอดเพื่อปล่อยแอนติเจนในสำลี
4. ดึงสำลีออกโดยบีบหัวสำลีกับด้านในของหลอดดูดขณะที่ดึงออก เพื่อไล่ของเหลวออกจากสำลีให้ได้มากที่สุด ทิ้งสำลีตามโปรโตคอลการกำจัดขยะอันตรายทางชีวภาพของคุณ
5. ใส่ปลายหยดไว้ด้านบนของหลอดสกัด วางตลับทดสอบบนพื้นผิวที่สะอาดและเรียบ
6. หยดสารละลาย 2 หยด (ประมาณ 65 μL) ลงในช่องตัวอย่าง จากนั้นเริ่มจับเวลา อ่านผลลัพธ์ที่แสดงภายใน 20-30 นาที และผลลัพธ์ที่อ่านหลังจาก 30 นาทีจะไม่ถูกต้อง
การตีความผลลัพธ์
| เชิงลบ ผลลัพธ์: |
มีเส้นสีหนึ่งเส้นปรากฏขึ้นในบริเวณเส้นควบคุม (C) ไม่มีเส้นปรากฏขึ้นในบริเวณทดสอบ (T) ผลลบบ่งชี้ว่าไม่มีแอนติเจน SARS-CoV-2 อยู่ในตัวอย่าง หรือมีแอนติเจนอยู่ต่ำกว่าระดับที่ตรวจพบได้ของการทดสอบ
เชิงบวกผลลัพธ์:
ปรากฏเส้นสองเส้น เส้นสีหนึ่งเส้นควรอยู่ในบริเวณควบคุม (C) และเส้นสีที่ปรากฏอีกเส้นหนึ่งควรอยู่ในบริเวณทดสอบ (T) ผลเป็นบวกบ่งชี้ว่าตรวจพบ SARS-CoV-2 ในตัวอย่าง
ผลลัพธ์ไม่ถูกต้อง:
เส้นควบคุมไม่ปรากฏ สาเหตุที่เป็นไปได้มากที่สุดของความล้มเหลวของเส้นควบคุมคือปริมาณตัวอย่างที่ไม่เพียงพอหรือเทคนิคขั้นตอนที่ไม่ถูกต้อง โปรดตรวจสอบขั้นตอนและทำการทดสอบซ้ำด้วยชุดทดสอบใหม่ หากปัญหายังคงอยู่ ให้หยุดใช้ชุดทดสอบทันทีและติดต่อตัวแทนจำหน่ายในพื้นที่ของคุณ
บันทึก:
ความเข้มของสีในบริเวณเส้นทดสอบ (T) จะแตกต่างกันไปขึ้นอยู่กับความเข้มข้นของแอนติเจน SARS-CoV-2 ที่มีอยู่ในตัวอย่าง ดังนั้น เฉดสีใดๆ ในบริเวณเส้นทดสอบ (T) ควรได้รับการพิจารณาว่าเป็นบวก
การควบคุมคุณภาพ
- การทดสอบนี้ประกอบด้วยการควบคุมตามขั้นตอน เส้นสีที่ปรากฏในบริเวณควบคุม (C) ถือเป็นการควบคุมตามขั้นตอนภายใน ยืนยันว่ามีการซึมผ่านของเมมเบรนเพียงพอ
- ชุดนี้ไม่ได้จัดส่งมาตรฐานควบคุมมาให้ แต่ขอแนะนำให้ทดสอบการควบคุมเชิงบวกและเชิงลบเป็นแนวทางปฏิบัติที่ดีของห้องปฏิบัติการ เพื่อยืนยันขั้นตอนการทดสอบและตรวจยืนยันประสิทธิภาพการทดสอบที่เหมาะสม
ข้อจำกัดของการทดสอบ
- ตลับทดสอบแบบรวดเร็วสำหรับแอนติเจน SARS-CoV-2 มีไว้สำหรับการวินิจฉัยในหลอดทดลองโดยผู้เชี่ยวชาญเท่านั้น ควรใช้การทดสอบนี้เพื่อตรวจหาแอนติเจน SARS-CoV-2 ในสำลีเช็ดช่องปากและคอหอย ไม่สามารถระบุค่าเชิงปริมาณหรืออัตราการเพิ่มขึ้นของความเข้มข้นของ SARS-CoV-2 ได้จากการทดสอบเชิงคุณภาพนี้
- ความแม่นยำของการทดสอบขึ้นอยู่กับคุณภาพของตัวอย่างไม้พันสำลี อาจเกิดผลลบปลอมได้จากการเก็บตัวอย่างที่ไม่เหมาะสม
- ตลับทดสอบแบบรวดเร็วสำหรับแอนติเจน SARS-CoV-2 จะระบุการมีอยู่ของ SARS-CoV-2 ในตัวอย่างจากทั้งสายพันธุ์ของไวรัสโคโรนา SARS-CoV-2 ที่มีชีวิตและไม่มีชีวิตเท่านั้น
- เช่นเดียวกับการทดสอบการวินิจฉัยทั้งหมด ผลลัพธ์ทั้งหมดจะต้องได้รับการตีความร่วมกับข้อมูลทางคลินิกอื่นๆ ที่แพทย์ทราบ
- ผลลบที่ได้จากชุดนี้ควรได้รับการยืนยันด้วย PCR อาจได้ผลลัพธ์ลบหากความเข้มข้นของ SARS-CoV-2 ที่อยู่ในสำลีไม่เพียงพอหรือต่ำกว่าระดับที่ตรวจพบได้จากการทดสอบ
- เลือดหรือเมือกส่วนเกินบนตัวอย่างสำลีอาจรบกวนประสิทธิภาพการทำงานและอาจทำให้ผลเป็นบวกปลอมได้
- ผลบวกของ SARS-CoV-2 ไม่ได้ขัดขวางการติดเชื้อร่วมกับเชื้อก่อโรคอับละอองเกสร ดังนั้นจึงควรพิจารณาความเป็นไปได้ของการติดเชื้อแบคทีเรียโดยตรง
- ผลลบไม่ได้ตัดความเป็นไปได้ของการติดเชื้อ SARS-CoV-2 โดยเฉพาะในผู้ที่สัมผัสกับเชื้อไวรัส ควรพิจารณาการตรวจติดตามผลด้วยการวินิจฉัยทางโมเลกุลเพื่อตัดความเป็นไปได้ของการติดเชื้อในบุคคลเหล่านี้
- ผลลัพธ์เชิงบวกอาจเกิดจากการติดเชื้อไวรัสโคโรนาสายพันธุ์ที่ไม่ใช่ SARS-CoV-2 ในปัจจุบัน เช่น ไวรัสโคโรนา HKU1, NL63, OC43 หรือ 229E
- ผลการทดสอบแอนติเจนไม่ควรใช้เป็นเพียงพื้นฐานในการวินิจฉัยหรือแยกแยะการติดเชื้อ SARS-CoV-2 หรือเพื่อแจ้งสถานะการติดเชื้อ
- สารเคมีสกัดมีคุณสมบัติในการฆ่าเชื้อไวรัสได้ แต่ไม่สามารถทำให้ไวรัสไม่ทำงานได้ 100% วิธีการทำให้ไวรัสไม่ทำงานสามารถดูได้จาก: วิธีที่ WHO/CDC แนะนำ หรือสามารถดำเนินการตามกฎระเบียบในท้องถิ่นได้
ลักษณะการทำงาน
ความไวและความเฉพาะเจาะจง
ชุดทดสอบแบบรวดเร็วแอนติเจน SARS-CoV-2 ได้รับการประเมินด้วยตัวอย่างที่ได้จากผู้ป่วย โดยใช้ PCR เป็นวิธีอ้างอิงสำหรับชุดทดสอบแบบรวดเร็วแอนติเจน SARS-CoV-2 ตัวอย่างจะถือว่าเป็นผลบวกหากผล PCR บ่งชี้ว่าเป็นบวก
| วิธี | อาร์ที-พีซีอาร์ | ผลลัพธ์ทั้งหมด | ||
| ตลับทดสอบแบบรวดเร็วสำหรับแอนติเจน SARS-CoV-2 | ผลลัพธ์ | เชิงบวก | เชิงลบ | |
| เชิงบวก | 38 | 3 | 41 | |
| เชิงลบ | 2 | 360 | 362 | |
| ผลลัพธ์ทั้งหมด | 40 | 363 | 403 | |
ความไวสัมพัทธ์: 95.0% (95%CI*: 83.1%-99.4%)
ความจำเพาะสัมพันธ์: 99.2% (95%CI*: 97.6%-99.8%)
*ช่วงความเชื่อมั่น
ขีดจำกัดการตรวจจับ
เมื่อปริมาณไวรัสมากกว่า 400TCID50/มล. อัตราการตรวจพบผลบวกมากกว่า 95% เมื่อปริมาณไวรัสน้อยกว่า 200TCID50/มล. อัตราการตรวจจับผลบวกน้อยกว่า 95% ดังนั้นขีดจำกัดการตรวจจับขั้นต่ำของผลิตภัณฑ์นี้คือ 400TCID50/มล.
ความแม่นยำ
ทดสอบตัวอย่างน้ำยาสามชุดติดต่อกันเพื่อความแม่นยำ โดยใช้ตัวอย่างน้ำยาชุดต่างๆ ทดสอบตัวอย่างเดียวกันที่ผลเป็นลบ 10 ครั้งติดต่อกัน และผลออกมาเป็นลบทั้งหมด ส่วนตัวอย่างน้ำยาชุดต่างๆ ทดสอบตัวอย่างบวกชุดเดียวกัน 10 ครั้งติดต่อกัน และผลออกมาเป็นบวกทั้งหมด
เอฟเฟกต์ HOOK
เมื่อปริมาณไวรัสในตัวอย่างที่ต้องการทดสอบถึง 4.0*105ทีซีไอดี50/ml ผลการทดสอบยังไม่แสดงผล HOOK
ปฏิกิริยาข้าม
มีการประเมินปฏิกิริยาข้ามของชุดทดสอบ ผลปรากฏว่าไม่มีปฏิกิริยาข้ามกับตัวอย่างต่อไปนี้
| ชื่อ | ความเข้มข้น |
| เอชซีโอวี-เอชเคยู1 | 105ทีซีไอดี50/มล. |
| สแตฟิโลค็อกคัส ออเรียส | 106ทีซีไอดี50/มล. |
| สเตรปโตค็อกคัสกลุ่มเอ | 106ทีซีไอดี50/มล. |
| ไวรัสหัด | 105ทีซีไอดี50/มล. |
| ไวรัสคางทูม | 105ทีซีไอดี50/มล. |
| อะดีโนไวรัสชนิดที่ 3 | 105ทีซีไอดี50/มล. |
| โรคปอดบวมจากไมโคพลาสมา | 106ทีซีไอดี50/มล. |
| พาราอิมฟลูเอนซาไวรัสชนิดที่ 2 | 105ทีซีไอดี50/มล. |
| ไวรัสเมตาพนิวโมของมนุษย์ | 105ทีซีไอดี50/มล. |
| ไวรัสโคโรนาในมนุษย์ OC43 | 105ทีซีไอดี50/มล. |
| ไวรัสโคโรนาสายพันธุ์ 229E ในมนุษย์ | 105ทีซีไอดี50/มล. |
| บอร์เดเทลลา พาราเพอร์ทูซิส | 106ทีซีไอดี50/มล. |
| ไข้หวัดใหญ่สายพันธุ์ B วิกตอเรีย | 105ทีซีไอดี50/มล. |
| ไข้หวัดใหญ่สายพันธุ์ B | 105ทีซีไอดี50/มล. |
| ไข้หวัดใหญ่สายพันธุ์ A H1N1 2009 | 105ทีซีไอดี50/มล. |
| ไข้หวัดใหญ่ชนิด A H3N2 | 105ทีซีไอดี50/มล. |
| H7N9 | 105ทีซีไอดี50/มล. |
| ไข้หวัดนก H5N1 | 105ทีซีไอดี50/มล. |
| ไวรัสเอปสเตน-บาร์ | 105ทีซีไอดี50/มล. |
| เอนเทอโรไวรัส CA16 | 105ทีซีไอดี50/มล. |
| ไรโนไวรัส | 105ทีซีไอดี50/มล. |
| ไวรัส RSV | 105ทีซีไอดี50/มล. |
| สเตรปโตค็อกคัส นิวโมนิ-เออี | 106ทีซีไอดี50/มล. |
| แคนดิดา อัลบิแคนส์ | 106ทีซีไอดี50/มล. |
| คลามีเดีย นิวโมเนีย | 106ทีซีไอดี50/มล. |
| โรคไอกรนชนิดบอร์เดเทลลา | 106ทีซีไอดี50/มล. |
| ปอดอักเสบจากเชื้อนิวโมซิสติส จิโรเวซิ | 106ทีซีไอดี50/มล. |
| ไมโคแบคทีเรียม ทูเบอร์คูโลซิส | 106ทีซีไอดี50/มล. |
| ลีจิโอเนลลา นิวโมฟิลา | 106ทีซีไอดี50/มล. |
Iสารรบกวน
ผลการทดสอบจะไม่ถูกรบกวนจากสารที่ความเข้มข้นต่อไปนี้:
| การแทรกแซง สาร | คอน | สารรบกวน | คอน |
| เลือดทั้งหมด | 4% | เจลเบนโซอินผสม | 1.5 มก./มล. |
| ไอบูโพรเฟน | 1มก./มล. | โครโมลินไกลเคต | 15% |
| เตตราไซคลิน | 3ug/มล. | คลอแรมเฟนิคอล | 3ug/มล. |
| มิวซิน | 0.5% | มูพิโรซิน | 10 มก./มล. |
| เอริโทรไมซิน | 3ug/มล. | โอเซลทามิเวียร์ | 5 มก./มล. |
| โทบราไมซิน | 5% | ยาหยอดจมูกนาฟาโซลีนไฮโดรคลอไรด์ | 15% |
| เมนทอล | 15% | สเปรย์ฟลูติคาโซนโพรพิโอเนต | 15% |
| อาฟริน | 15% | ดีออกซีอิพิเนฟรินไฮโดรคลอไรด์ | 15% |
บรรณานุกรม
1.Weiss SR, Leibowitz JZ. การเกิดโรคโคโรนาไวรัส Adv Virus Res 2011;81:85-164
2.Cui J,Li F,Shi ZL.ต้นกำเนิดและวิวัฒนาการของไวรัสโคโรนาที่ก่อโรค Nat Rev Microbiol 2019;17:181-192
3. Su S, Wong G, Shi W และคณะ ระบาดวิทยา การรวมตัวทางพันธุกรรม และการเกิดโรคของไวรัสโคโรนา TrendsMicrobiol 2016;24:490-502